Anemia da doença inflamatória
A Anemia da Doença Inflamatória (ADI) é uma causa comum de anemia na prática veterinária de rotina. Na maioria das vezes apresenta-se leve a moderada, normocítica, normocrômica e não regenerativa. Está associada a vários distúrbios crônicos, incluindo doenças infecciosas, inflamatórias, imunomediadas e neoplásicas.Embora esse tipo de anemia também tenha sido chamado de “anemia de doença crônica (ADC)”, não existe consenso em relação à terminologia.
ADI é caracterizada por três fatores fisiopatológicos principais: tempo de vida reduzido dos eritrócitos, inibição do metabolismo do ferro e comprometimento da resposta da medula óssea à eritropoietina.
– Tempo de vida eritrocitária reduzida: além da presença de uma eritropoese um pouco ineficaz, a redução da expectativa de vida média dos eritrócitos foi sugerida por alguns autores através de uma base imunológica, onde os macrófagos são ativados devido a várias citocinas inflamatórias liberadas durante a inflamação. Isso acelera a eliminação dos eritrócitos da circulação via eritrofagocitose pelos macrófagos teciduais. Essa eritrofagocitose é ainda acelerada por imunoglobulinas que revestem os eritrócitos.
– Inibição do metabolismo de Ferro: Acredita-se que esta mudança seja parte de uma importante resposta imunológica do hospedeiro para limitar o acesso microbiano ao ferro e resulta da supressão da absorção gastrintestinal de ferro e aumento da retenção de ferro nos macrófagos envolvidos na inflamação. Uma vez que a liberação de ferro dos macrófagos é bloqueada, a concentração sérica de ferro diminui rapidamente e, como resultado, o suprimento de ferro para a síntese de hemoglobina na medula óssea é reduzido e a eritropoese é suprimida. Este é um mecanismo importante que desencadeia o desenvolvimento da ADI.
– Comprometimento da medula óssea – eritropoietina: Esta eritropoiese defeituosa resulta de várias citocinas inflamatórias induzindo a resposta de eritropoietina prejudicada, juntamente com toxicidade direta nas células precursoras eritróides. Mecanismos subjacentes podem incluir indução de apoptose mediada por citocinas, regulação negativa da expressão do receptor de eritropoietina nas células progenitoras eritróides, expressão reduzida de outros fatores pró-hematopoiéticos, como fator de célula tronco e número reduzido de unidades formadoras de colônias eritróides.
Exames Laboratoriais:
Como a ADI é, na verdade, um estado “funcional” de deficiência de ferro, ela compartilha algumas características clínicas com outras causas de anemia, incluindo hipoferremia e uma variedade de alterações na morfologia eritrocitária. Por isso uma combinação de história clínica, exame físico e exames laboratoriais de rotina são, portanto, importantes para o diagnóstico de ADI. Contudo, uma vez que as doenças subjacentes conduzem a uma variedade de outras alterações hematológicas, o diagnóstico final da ADI deve ser feito após a exclusão de outras causas de anemia, como deficiências nutricionais, hipotiroidismo, mielodisplasia, reacções medicamentosas, doença renal crónica e hemorragia. Como não há informações sobre como esses parâmetros mudam no processo de ADI, especialmente a deficiência aguda de ferro e o efeito das doenças de base, o diagnóstico permanece difícil.
Tratamento:
Embora a ADI seja uma das causas mais comuns de anemia, raramente é grave o suficiente para exigir tratamento. Importante, e sempre que possível, o tratamento da doença subjacente desencadeando a inflamação deve ser introduzido antes de qualquer tratamento específico para a anemia. Em algumas doenças crônicas, como a neoplasia maligna, o tratamento curativo é muitas vezes impossível e, nesses casos, o tratamento da ADI (incluindo transfusões de sangue, terapia com ferro parenteral e administração de eritropoietina humana recombinante) poderia melhorar o resultado.

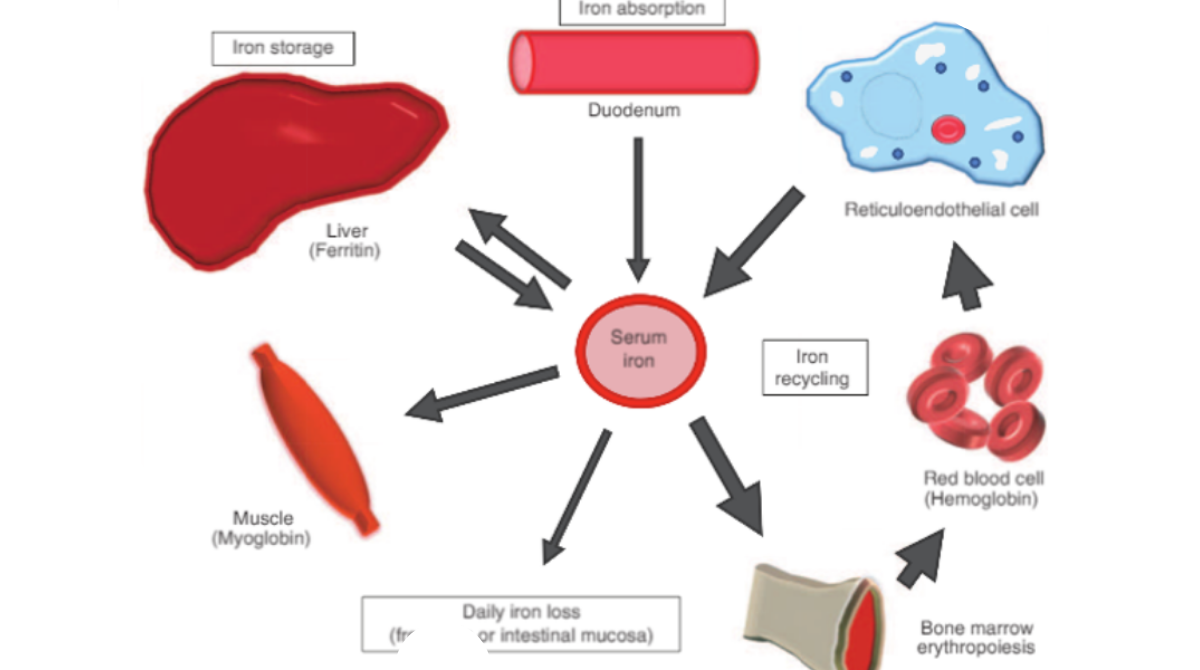
FIGURA 1 . Visão geral do metabolismo do ferro em mamíferos. A quantidade de absorção de ferro dos alimentos é extremamente pequena (1 a 2 mg / dia em adultos humanos) e é aproximadamente igual à perda diária de ferro. A maior parte do ferro necessário para a hematose é derivada da hemoglobina reciclada dos eritrócitos envelhecidos, através da eritrofagocitose realizada pelas células reticuloendoteliais. O excesso de ferro é armazenado principalmente no fígado como ferritina e liberado na circulação conforme necessário.
Fonte: Chikazawa S., Dunning MD. – A review of anaemia of inflammatory disease in dogs and cats. J Small Anim Pract. 2016 Jul;57(7):348-53. doi: 10.1111/jsap.12498.
Qualquer dúvida, estaremos a disposição!!
DIAG & VET – Laboratório veterinário de Análise Clínicas.
